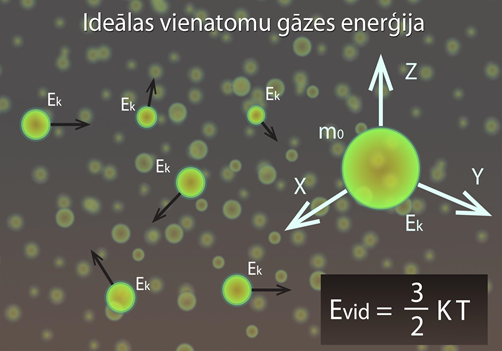
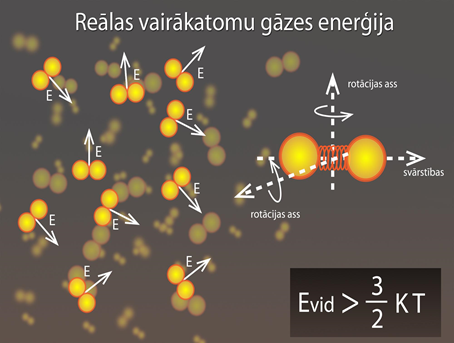
Par molekulāri kinētisko teoriju (MKT) sauc teoriju, kas izskaidro procesus, pamatojoties uz priekšstatu, ka viela sastāv no atomiem un molekulām, kas nepārtraukti haotiski kustas. MKT pamato trīs pieņēmumi:
1) jebkura viela sastāv no sīkām daļiņām – molekulām vai atomiem (1. att. a);
2) starp vielas daļiņām vienlaikus darbojas savstarpējas pievilkšanās un atgrūšanās spēki (1. att. b);
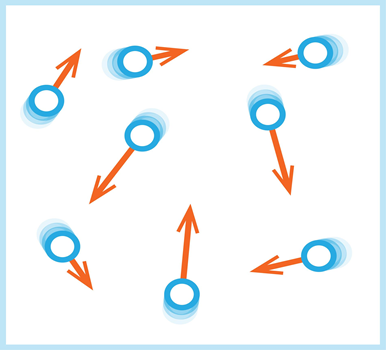
3) vielas daļiņas atrodas nepārtrauktā haotiskā kustībā (siltumkustībā) (1. att. c).
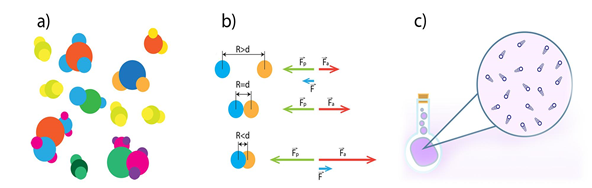
1.att. Molekulāri kinētiskās teorijas pamatpieņēmumu ilustrācija
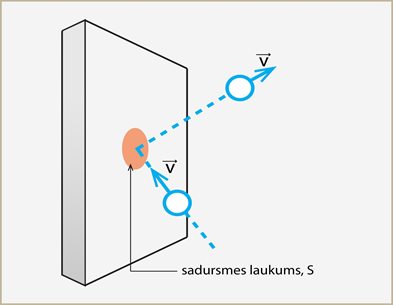
Jau pats nosaukums „kinētiskā teorija” nosaka, ka tiek aplūkota gāzes daļiņu kustība, jo vārds kinētika ir cēlies no sengrieķu vārda ‘kinētikos’, kas nozīmē „ar kustību saistīts”. Gāzes daļiņas, kustoties kādā noslēgtā tilpumā, ik pa laikam saduras ar trauka sieniņām un rada spiedienu, kā tas jau tika noskaidrots sadaļā par gāzes fizikālajiem parametriem. Gāzes spiedienu noslēgtā sistēmā nosaka šādi raksturlielumi:
1) gāzes daļiņu masa,
2) gāzes daļiņu ātrums,
3) gāzes daļiņu skaits.
Pirmkārt, spiediens ir atkarīgs no tā, cik smagas daļiņas kustas tilpumā (2. att.). Ja ātrums visām daļiņām ir vienāds, lielāku spiedienu uz trauka sieniņām rada smagākā daļiņa.
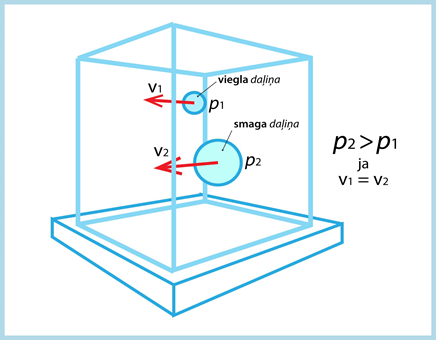
2.att. Daļiņu radītais spiediens ir atkarīgs no to masas
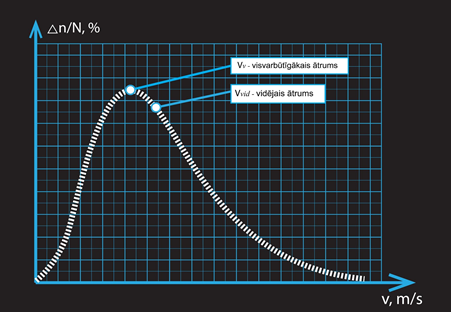
Daļiņas veidotā spiediena lielumu nosaka arī ātrums. Ja vieglāka daļiņa kustēsies ātrāk nekā smagāka (3. att.), tad tā var radīt lielāku spiedienu, ja ir pietiekošs ātruma pārsvars. Savukārt ja smagākai daļiņai ir lielāks ātrums, tas nozīmē, ka tās radītā spiediena lielumu nosaka ne tikai masas, bet arī ātruma atšķirības.
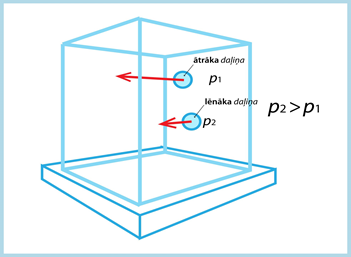
3.att. Daļiņu radītais spiediens ir atkarīgs no to ātruma
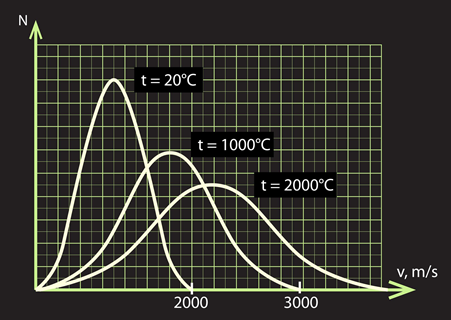
Vēl viens nozīmīgs spiedienu noteicošs faktors ir daļiņu skaits. Ir teiciens – „viens nav karotājs”, un to var attiecināt arī uz spiedienu. Ja tilpumā kustas maz daļiņu, tad spiediens ir attiecīgi mazāks nekā gadījumā, ja daļiņu skaits ir liels.