Siltuma daudzums
Iekšējā enerģija un temperatūra
Enerģiju, ko nosaka sistēmas daļiņu kustība un mijiedarbība, sauc par šīs sistēmas iekšējo enerģiju (skatīt nodaļu ''Iekšējā enerģija'').
Lai aprēķinātu kādas sistēmas iekšējo enerģiju, ir jāzina sistēmas uzbūve (mikrostruktūra), sistēmas daļiņu kustības un mijiedarbības raksturs. Aplūkojot siltumparādības un procesus pieņem, ka iekšējā enerģija ir atkarīga tikai no vielas daļiņu - molekulu (atomu) termiskās kustības un to savstarpējās mijiedarbības, neaplūkojot, piemēram, atoma kodolus veidojošo daļiņu mijiedarbību.
Pieņemsim, ka izolētā traukā, kuram ir šķērssiena, atdalītos tilpumos V1 un V2 dažādās temperatūrās atrodas gāze vai šķidrums (1. attēls). Šāds trauks ir it kā divas atsevišķas termodinamiskas sistēmas, kuru kopējā iekšējā enerģija (U) nemainās: U=U1+U2=const.
1.att.
Taču abas sistēmas neatrodas savstarpējā siltuma (termiskajā) līdzsvarā, jo to temperatūras ir atšķirīgas, un tāpēc tās var savstarpēji iedarboties caur šķērssienu - iekšējo enerģiju apmaiņa tomēr notiek, līdz iestājas siltuma līdzsvars un temperatūra izlīdzinās (kādēļ tā, skatīt nodaļās ''Siltumkustība un temperatūra'' un ''Otrais termodinamikas likums'').
Tā, piemēram, 2. attēlā redzams, ka telpā ienesta glāze ar karstu ūdeni, kura temperatūra ir augstāka nekā telpas temperatūra, atdziest - siltums no glāzes aizplūst apkārtējā telpā. Tas notiks līdz brīdim, kad telpas un glāzes temperatūras kļūs vienādas.
2.att.
Viena sistēma enerģiju ΔU atdod (tagad: U1 - ΔU), bet otra sistēma tikpat daudz enerģijas saņem (tagad: U2+ΔU).
Siltuma daudzums un siltumapmaiņa
Procesu, kurā notiek iekšējās enerģijas izmaiņa, nepastrādājot mehānisko darbu, sauc par siltumapmaiņu jeb siltuma pārnesi.
Ir trīs siltuma pārneses veidi: siltumvadīšana, kad siltums pāriet no siltāka ķermeņa (vai tā daļas) uz aukstāku ķermeni šo ķermeņu tiešā kontaktā (skatīt nodaļu ''Siltumvadīšana''), konvekcija — siltumapmaiņa, pārvietojoties vielai ar dažādu temperatūru (skatīt nodaļu ''Konvekcija'') un siltumstarojums, kad enerģiju pārnes elektromagnētiskie viļņi — termiskais starojums (skatīt nodaļu ''Siltuma starojums'').
Ja ķermenis uzņem vai atdod siltumenerģiju, tad tā iekšējā enerģija palielinās vai samazinās.
Tā rezultātā ķermeņa temperatūra paaugstinās vai pazeminās, var arī notikt agregātstāvokļa maiņa.
Dabā un sadzīvē bieži notiek vairāku ķermeņu siltumapmaiņa – vieni ķermenis siltumenerģiju saņem, bet citi atdod.
Iekšējās enerģijas daudzumu, ko ķermenis iegūst vai zaudē siltumapmaiņas procesā, sauc par siltuma daudzumu (Q).
Tā kā siltuma daudzums ir enerģija, [Q]=J
Saskaņā ar pirmo termodinamikas likumu Q=ΔU+A (skatīt nodaļu ''Pirmais termodinamikas likums''), ja sistēma ir noslēgta un netiek veikts mehāniskais darbs, siltumapmaiņas procesā vienu (piemēram sasilušo) ķermeņu iekšējā enerģija palielinās tieši par tik, par cik samazinās otru (piemēram, atdzisušo) ķermeņu iekšējā enerģija.
Tātad: Q=ΔU
Sistēma, kas siltuma daudzumu jeb siltumu Q atdod, ir ''karstāka'', bet sistēma, kas to saņem, — ''aukstāka''. Ja ķermenis siltuma daudzumu saņem, šo siltuma daudzumu uzskata par pozitīvu, ja atdod – par negatīvu.
Tātad, ja starp ķermeņiem, kas veido izolētu sistēmu, notiek tikai siltumapmaiņa, tad, saskaņā ar pirmo termodinamikas likumu, ķermeņu atdotais siltuma daudzums QA un citu ķermeņu saņemtais siltuma daudzums QS ir skaitliski vienādi: QA=QS
Ķermeņi, kuri atdziest un/vai kondensējas un/vai sacietē noteiktu siltuma daudzumu atdod, bet citi ķermeņi, kuri sasilst un/vai kūst un/vai iztvaiko, šo siltuma daudzumu saņem.
Ir jāņem vērā visu siltumapmaiņā piedalījušos ķermeņu temperatūras un/vai agregātstāvokļu izmaiņa.
Jāpiebilst, ka jēdziens ''siltuma daudzums'' nozīmē iekšējās enerģijas izmaiņu, bet ne iekšējās enerģijas daudzumu vispār. Dažkārt ikdienā sastopamajai frāzei, ka ''ķermenis satur noteiktu siltuma daudzumu'', nav fizikālas jēgas. Ķermenim var ''atņemt'' vai ''piešķirt'' noteiktu siltuma daudzumu, bet ķermenī siltuma daudzuma kā tāda nav.
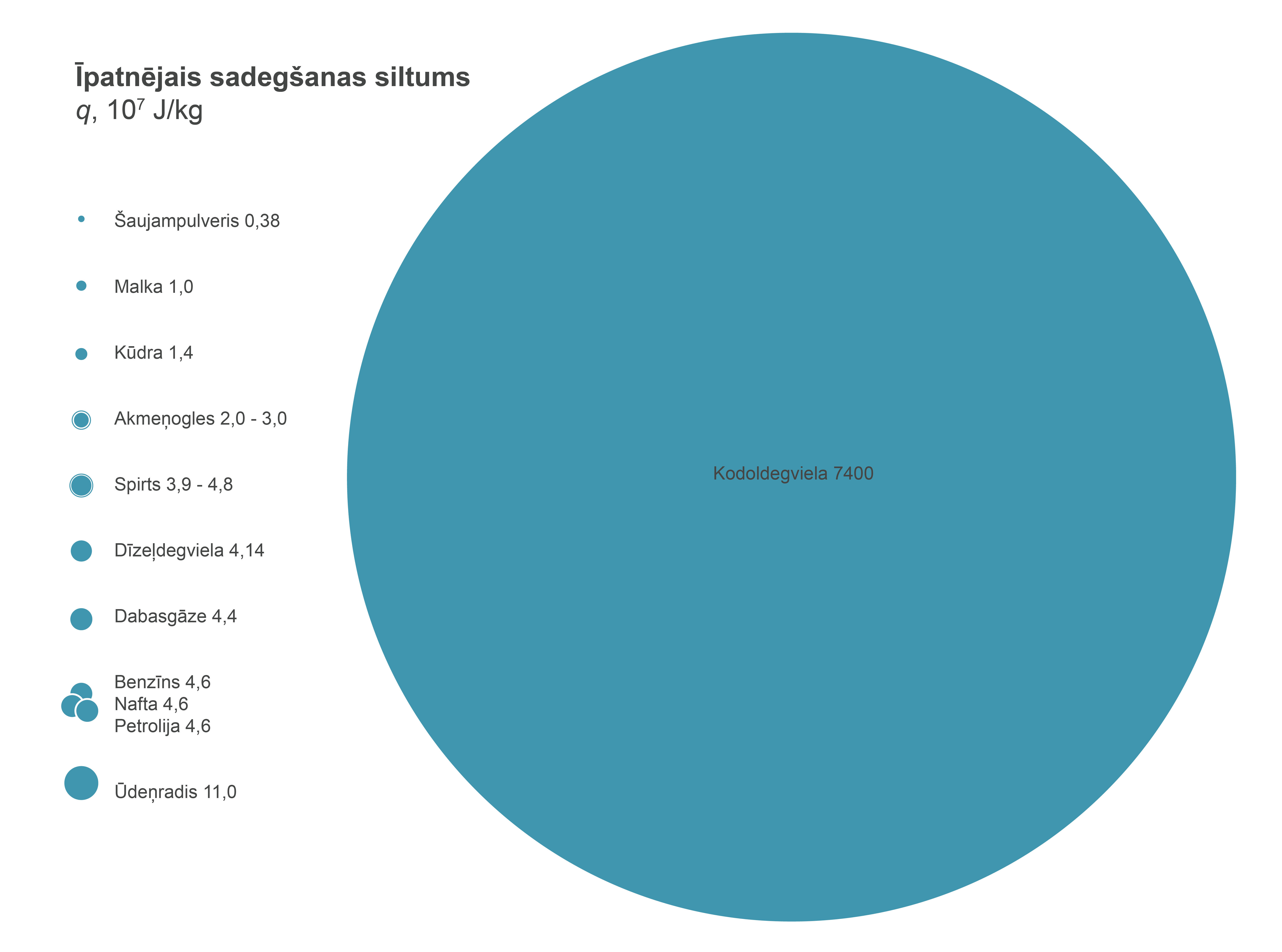
Siltuma daudzumu ķermeņi var saņemt gan notiekot siltuma apmaiņai noslēgtā sistēmā, kad vieni ķermeņi siltumu atdod, citi saņem, gan arī no sildītāja - parasti siltumam izdaloties eksotermiskās ķīmiskās reakcijās (kurināmajam sadegot - skatīt nodaļu ''Kurināmā sadegšana'') vai no elektriskajiem sildītājiem.
Lai gan siltuma daudzuma SI mērvienība ir džouli (J), sadzīvē bieži tiek lietota vēl viena mērvienība – kalorija (cal). Viena kalorija ir 4,19 J jeb 1J = 0,24 cal. Kalorija ir siltuma daudzums, kas nepieciešams, lai vienu gramu ūdens sasildītu par vienu Celsija grādu.