Zīmējumā attēlota nemainīgas masas gāzes tilpuma atkarība no absolūtās temperatūras. Gāze pāriet no stāvokļa 1 stāvoklī 2 un 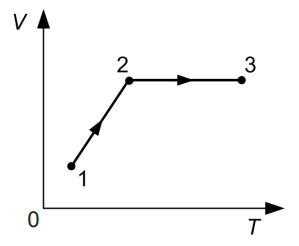 no stāvokļa 2 stāvoklī 3.
no stāvokļa 2 stāvoklī 3.
Grafiski attēlo gāzes spiediena atkarību no tilpuma! Grafikā norādi gāzes stāvokļus 1, 2 un 3!
Uzdevuma zīmējumā attēlotajā posms 1-2 atbilst izobāriskajām procesam. To var secināt pēc tā, ka gāzes tilpuma \(V\) atkarība no  gāzes absolūtās temperatūras \(T\) ir tiešā proporcionalitāte. Tātad, posmā 1-2 gāzes spiediens \(p\) nemainās, bet gāzes absolūtā temperatūra \(T\) un gāzes tilpums \(V\) pieaug.
gāzes absolūtās temperatūras \(T\) ir tiešā proporcionalitāte. Tātad, posmā 1-2 gāzes spiediens \(p\) nemainās, bet gāzes absolūtā temperatūra \(T\) un gāzes tilpums \(V\) pieaug.
Posmā 2-3, absolūtai gāze temperatūrai \(T\) pieaugot, gāzes tilpums \(V\) nemainās. Tādu procesu sauc par izohorisku. Izohoriskajā procesā gāzes spiediens \(p\) un gāzes absolūtā temperatūra \(T\) ir tieši proporcionāli lielumi, tātad, paaugstinoties gāzes absolūtai temperatūrai \(T\), paaugstinās arī gāzes spiediens \(p\).
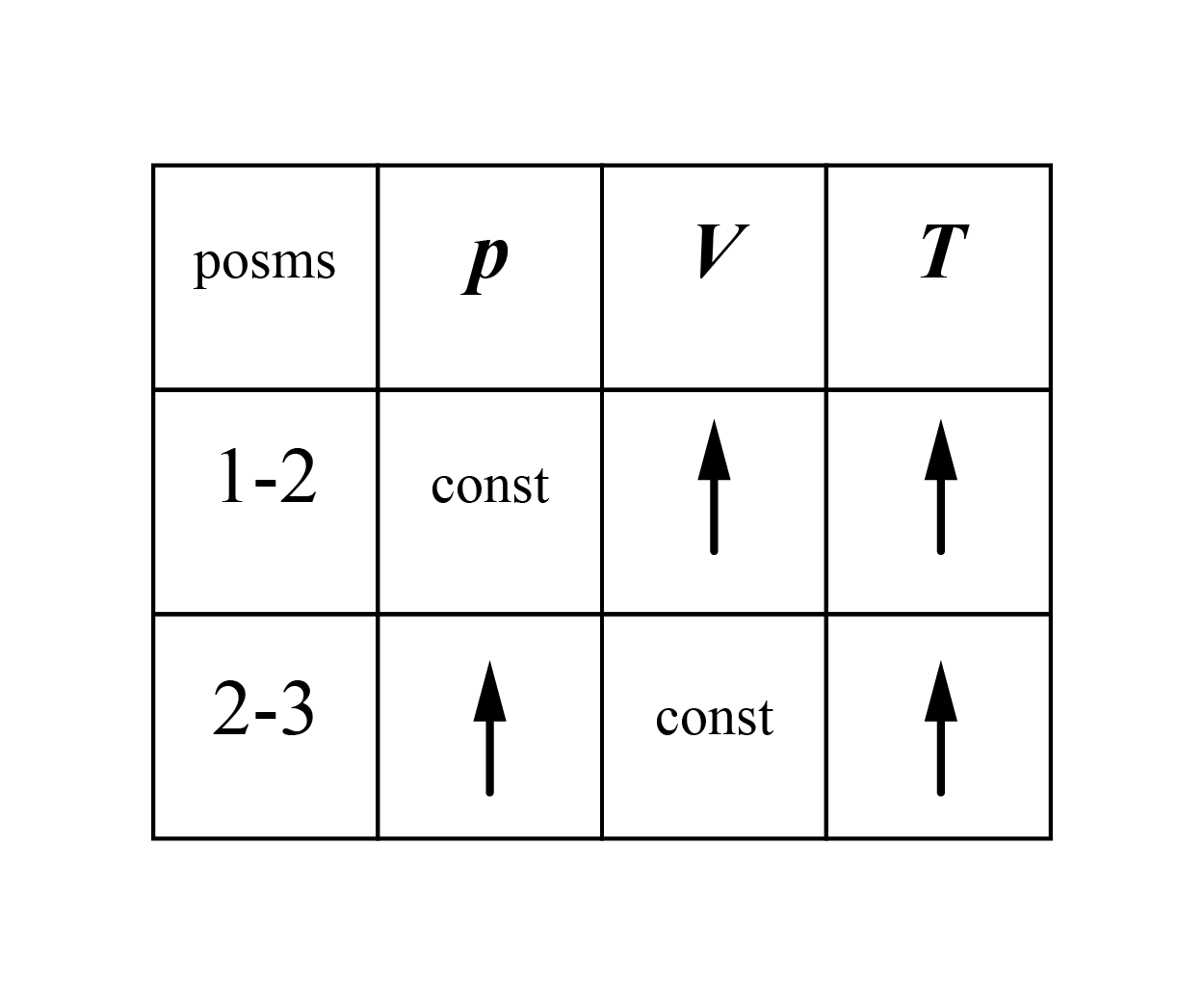
Informāciju par augstāk aprakstītajiem procesiem var apkopot arī tabulā:
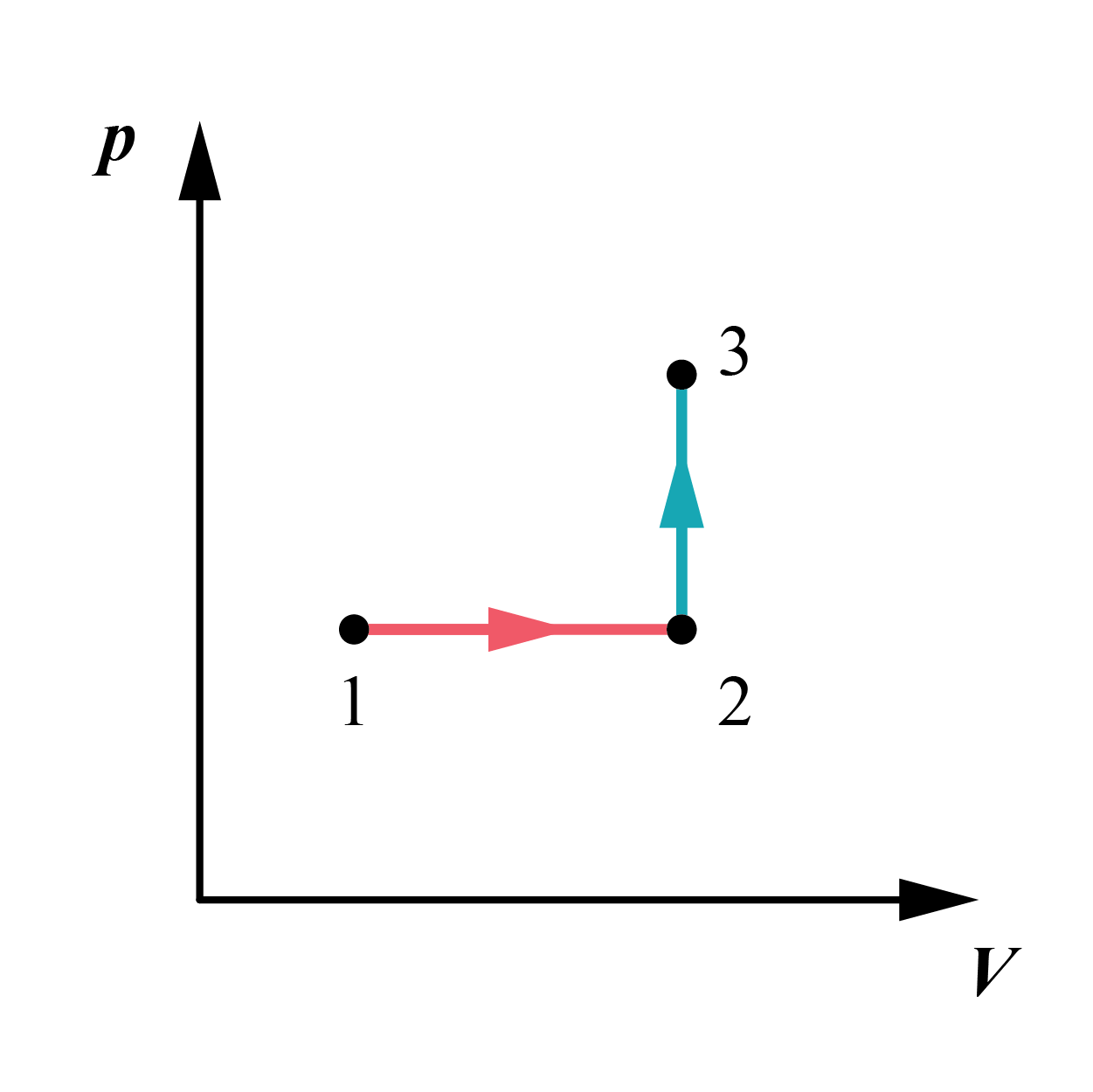
Attēlojot grafiski gāzes spiedienu \(p\) atkarībā no gāzes tilpuma \(V\) uzdevuma zīmējumā attēlotajiem procesiem, būs divi posmi:
posmā 1-2 gāze izobāriski izplēšas;
posmā 2-3 tilpums \(V\) nemainās, spiediens \(p\) pieaug.
Gāzes spiediena atkarība no tilpuma:
Vērtēšanas kritēriji
Abu posmu analizē secina, kā mainās katrs gāzes parametrs, mainoties temperatūrai – 1 punkts.
Attēlo prasītās koordinātās gāzes parametru maiņu, pieraksta gāzes stāvokļiem atbilstošos ciparus un posma virzienu – 1 punkts.